Doenças do Aparelho Digestivo
As principais doenças do aparelho digestivo, de tratamento cirúrgico, são aqui descritas. As informações são resumidas, outros detalhes podem ser solicitados através de contato.
ESÔFAGO
- Doença do Refluxo Gastroesofágico (DRGE)
- Neoplasias benignas
- Câncer do esôfago
Doença do refluxo gastroesofágico (DRGE)
A doença do refluxo é o resultado do fluxo retrógrado de parte do conteúdo gastroduodenal para o esôfago. Aumenta progressivamente após os 40 anos e em ambos os sexos. O principal sintoma é a pirose que é a sensação de queimação retroesternal e ocorre entre 30 e 60 minutos após a refeição, especialmente alimentação gordurosa, condimentada e ácida. A endoscopia digestiva alta é o principal exame para o diagnóstico, é capaz de avaliar a gravidade e fazer biópsias. A endoscopia pode também diagnosticar a hérnia de hiato que á a passagem da transição esofagogástrica (linha Z) acima do pinçamento diafragmático. A Ph-Metria de 24 horas pode ser indicada naquelas situações onde não se observa esofagite endoscópica. Um outra forma de diagnosticar a DRGE é o teste terapêutico (alívio dos sintomas com medicações para DRGE). Normalmente o tratamento é clínico. As medidas dietéticas (perder peso, alterar a alimentação), comportamentais, antiácidos, inibidores de receptores H2, inibidor de bomba de próton e procinético, apresentam bons resultados. A cirurgia está indicada para pacientes que não melhoram após o tratamento clínico bem realizado, pacientes com esofagite severa e hérnia de hiato maior que 3 cm, complicações da esofagite. A cirurgia é realizada por videolaparoscopia e consiste em recolocação do esôfago na cavidade abdominal, aproximação dos pilares do diafragma (hiatoplastia) e envolvimento do esôfago pelo fundo gástrico (fundoplicatura).
ESTÔMAGO
- Neoplasias benignas
- Câncer gástrico
Câncer gástrico
O câncer do estômago no Brasil é o segundo mais frequente em homens e o quarto em mulheres, sendo a segunda maior causa de óbito por neoplasia. Na maioria dos casos a doença é diagnosticada em estádio avançado e a sobrevida em cinco anos na doença localizada é superior a 50% enquanto que no paciente com metástase é 3%. O tipo histológico mais comum é o adenocarcinoma, representando mais de 80% dos casos.
Os principais sintomas observados são a dor abdominal, geralmente epigástrica, perda de peso, náusea, vômitos, anorexia, saciedade precoce e disfagia. Nos pacientes com doença avançada pode ser observado massa abdominal, linfonodo umbilical (Irmã Maria José), ascite (água no abdome), linfonodo supra-clavicular esquerdo (Virchow), fígado palpável e implante para o ovário em mulheres (tumor de Krukenberg). O diagnóstico é realizado através da endoscopia digestiva alta com biópsias múltiplas. Deve ser avaliada a localização do tumor no estômago, a extensão da doença e o grau de invasão na parede. A tomografia computadorizada de abdome deve ser realizada para verificar a presença de doença avançada (linfonodos, ascite, metástase hepática). Os marcadores tumorais CEA, CA 72.4 e CA 19-9 podem ser úteis no diagnóstico.
O tratamento consiste em gastrectomia total ou subtotal (dependendo da localização da lesão), associado à linfadenectomia (retirada dos linfonodos) regional. A quimioterapia está indicada e pode melhorar os resultados do tratamento cirúrgico. Os resultados do tratamento paliativo não são bons, com o paciente apresentando sobrevida curta, entretanto estão indicados em casos de obstrução e sangramento.
INTESTINO
- Apendicite aguda
- Câncer colo-retal
- Doença hemorroidária
Câncer colo-retal
O câncer colo-retal representa o quarto lugar entre os tumores malignos e é a segunda causa de morte previsível. Considerada uma doença tratável e frequentemente curável quando não acomete outros órgãos. Entre os fatores de risco temos a história familiar, dieta, álcool e fumo, obesidade, sedentarismo e idade acima de 50 anos. Algumas condições hereditárias como a polipose familiar e o câncer colo-retal hereditário sem polipose são também implicados.
Os sintomas observados são a história de constipação crônica, anemia, dor abdominal, massa abdominal, melena (fezes escurecidas com sangue), diarréia, fraqueza e tenesmo.
O diagnóstico é realizado através de colonoscopia com biópsia e estudo histopatológico. Por ser observada uma grande parte no reto-sigmóide, a reto-sigmoidoscopia com aparelho rígido tem sido muito empregado. Os pacientes com idade igual ou superior a 50 anos devem realizar o exame.
O tratamento é realizado através da cirurgia. Deve ser retirada parte do intestino grosso (colectomia) com o tumor envolvido e os linfonodos regionais (linfadenectomia). O tratamento com radioterapia associado a quimioterapia deve ser realizada para diminuir os índices de recidiva (retorno da doença). Naqueles com doença avançada (fora do local de origem), os resultados são menos otimistas.
A prevenção através de uma dieta rica em fibras, vegetais, frutas, cálcio e pobre em gordura animal, apresentam resultados animadores. Da mesma forma a prática de exercícios físicos contribui para a redução da prevalência da doença.
FÍGADO
As doenças cirúrgicas do fígado têm representado um percentual significativo das cirurgias do aparelho digestivo. As principais estão aqui representadas:
1. Doenças císticas do fígado
- Cisto simples não parasitário
- Doença policística
- Cisto hidático
- Cistoadenomas
- Cistoadenocarcinomas
2. Neoplasias
- Tumores benignos
- Hemangioma
- Hiperplasia nodular focal
- Adenoma hepatocelular
- Tumores malignos
- Primários
- Carcinoma hepatocelular
- Carcinoma fibrolamelar
- Colangiocarcinoma periférico
- Metástases
- Primários
3. Abscesso hepático
Hemangioma hepático
O hemangioma hepático é o tumor benigno mais comum do fígado, sendo observado em 2-7% da população geral. É mais comum em mulheres na relação de 5:1 a 6:1 e sua incidência é maior entre a 3ª e 5ª década de vida. Seu desenvolvimento pode ter alguma relação com níveis hormonais e a exposição a altos níveis de estrogênio e progesterona, tais como ocorrem na multiparidade, gestação e uso de contraceptivos orais, que pode ser a razão da frequência maior em mulheres. Entretanto sua patogênese ainda é controversa. O uso frequente da ultrassonografia abdominal e tomografia computadorizada para indicações variadas têm levado ao aumento no diagnóstico de hemangiomas hepáticos.
Sua etiologia não é completamente esclarecida, embora a anomalia congênita tenha sido suspeitada. Eles geralmente se originam da proliferação de células endoteliais vascular, aumentando de tamanho por ectasia ao invés de hiperplasia. Não existem relatos de transformação maligna do hemangiomas em acompanhamento em longo prazo.
O hemangioma hepático é normalmente assintomático e devido à ausência de sintomas o tamanho do hemangioma pode variar muito quando descobertos. O hemangioma aumenta de tamanho em 10-20% dos pacientes e, por ele ocupar espaço e deslocar outros órgãos, pode tornar-se sintomático apresentando dor no quadrante superior direito do abdome, náuseas e vômitos. Episódios de febre têm sido registrados naqueles pacientes com hemangiomas gigantes, como resultado de trombose e necrose no hemangioma. Hemangioma é definido como gigante quando apresenta tamanho igual ou superior a quatro centímetros. Outros sintomas incluem sensação de compressão abdominal leve ou até mesmo hemoperitôneo devido à ruptura do tumor. Apresentações incomuns como icterícia obstrutiva, cólica biliar, torção de lesão pediculada e compressão gástrica podem ser observadas. Complicações como trombose infarto e hemorragia têm sido registradas nos hemangiomas gigantes e responsáveis por dor aguda severa. A ruptura traumática ou espontânea de um hemangioma gigante é um achado incomum. Entretanto, quando presentes, a mortalidade é elevada neste grupo de pacientes.
A síndrome de Kasabach-Merritt é uma complicação rara, porém bem conhecida dos hemangiomas gigantes, que é caracterizada pela combinação de tumor vascular e coagulopatia de consumo. Estes pacientes podem apresentar trombocitopenia severa, baixos níveis de fibrinogênio e aumento dos produtos de degradação da fibrina, devido à fibrinólise secundária e hemólise microagiopática. O objetivo do tratamento nestes casos é retirar o hemangioma, tornando a síndrome reversível. Em crianças a presença de hemangiomas de pele no dorso e no tronco pode ser observado. Em algumas situações pode contribuir para o diagnóstico de tumoração hepática inespecífica.
Normalmente as provas de função hepática estão normais. Exames como bilirrubinas, fosfatase alcalina, gama GT, bem como AST e ALT, não apresentam manifestações que possam sugerir o diagnóstico. Da mesma forma os marcadores tumorais alfa-fetoproteina, CEA e CA 19-9 estão normais.
A ultrassonografia é geralmente usada como investigação diagnóstica de nódulos hepáticos. Na tomografia computadorizada de abdome com contraste, o hemangioma se apresenta normalmente como enchimento vascular centrípeto progressivo na fase arterial, na fase portal e na fase de equilíbrio (Figura 1). Na ressonância nuclear magnética (RNM) se apresenta como massa hipointensa em T1, massa hiperintensa em T2. Na fase arterial pós-contraste em T1 com intensificação nodular periférica enquanto que na fase venosa portal com enchimento centrípeto. Normalmente não há indicação de biópsia nesses pacientes, existe um risco relacionado ao sangramento intenso que pode ameaçar a vida do paciente.
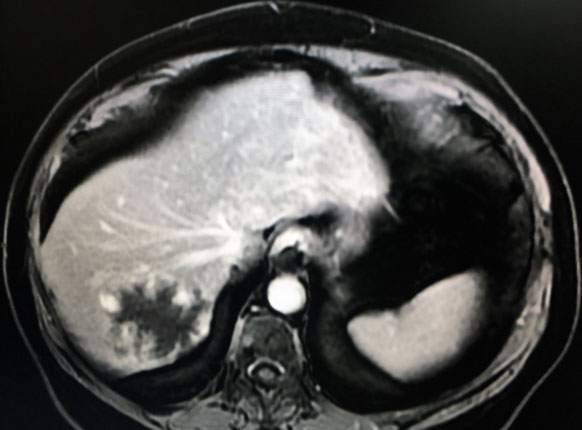
Figura 1. Tomografia com contraste evidenciando hemangioma em lobo hepático direito.
Como regra não há indicação de tratamento cirúrgico. Entre as opções de tratamento estão disponíveis para o hemangioma hepático podemos observar e fazer seguimento nos pacientes assintomáticos.
Indicação de cirurgia incluem pacientes com sintomas exuberantes, a coagulopatia de consumo da Síndrome de Kasabach-Merritt, a insuficiência cardíaca congestiva por hiperfluxo e a torção e ruptura em peritôneo livre.
A embolização transarterial pode ser aplicada para aliviar os sintomas do hemangioma hepático gigante, bem como nos casos de coagulação intravascular disseminada. Uma redução no tamanho do hemangioma é alcançada, porém a recorrência é comum devido à recanalização.
Quando o tratamento cirúrgico é necessário, a enucleação ou a ressecção, tanto por videolaparoscopia quanto por cirurgia aberta podem ser realizadas (Figura 2).
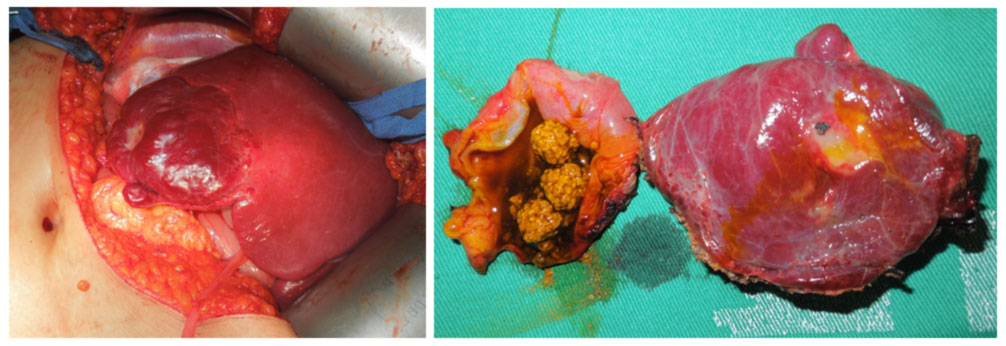
Figura 2. Raro caso de ressecção hepática em paciente com hemangioma no leito da vesícula biliar e colelitíase sintomática.
HIPERPLASIA NODULAR FOCAL
A Hiperplasia Nodular Focal (HNF) é considerada como um tumor hepatocitário benigno, sendo o segundo mais comum entre os tumores benignos do fígado, logo após o hemangioma. Seu achado é frequentemente incidental durante um exame de ultrassonografia, portanto assintomático em 80 a 90% dos casos. Tem prevalência estimada na população geral entre 0,9 a 3%, e sua incidência é preferencialmente no sexo feminino (8:1), na faixa etária entre 30 e 50 anos.
Malformações arteriais pré-existentes são responsáveis por uma resposta hiperplásica que originam a lesão. Esta desordem vascular pode explicar o aparecimento de leões em certas circunstâncias como síndrome de Budd-Chiari, Síndrome de Abernethy, doença de Rendu-Osler-Weber ou trombose portal com subsequente arterialização hepática.
Embora a maioria das pessoas acometidas pela HNF faça uso de contraceptivos orais, seu papel na formação destas lesões ainda não está muito bem esclarecido. A forma típica da HNF é usualmente encontrada como uma massa única solitária, bem circunscrita, não encapsulada e com presença de cicatriz central estrelada, de coloração branca acinzentada. Esta cicatriz central é encontrada em 50% dos nódulos da HNF, sendo sua presença, associada às outras características, um sinal patognomônico.
A HNF pode também ser encontrada em associação com outras lesões hepáticas. Há uma coexistência maior com hemangiomas (23%) e menor com adenomas (3,6%). A HNF pode ainda coexistir com doenças extrahepáticas tais como anomalias cerebrovasculares, anemias falciformes, displasias císticas do fígado, síndrome Kipple-Tranaunay, meningiomas e astrocitomas cerebrais.
A HNF é geralmente assintomática, entretanto, alguns pacientes podem manifestar uma dor abdominal vaga, não específica, como dispepsia, sensação de plenitude e desconforto epigástrico. Lesões pediculadas podem provocar dores agudas devido à sua torção.
Exames laboratoriais, incluindo testes de função hepática, são normais em 80% dos casos. Nos pacientes com grandes lesões e compressão extrínseca das vias biliares intrahepáticas, podem ser observadas elevações moderadas da Gama glutamil transpeptidase e fosfatase alcalina.
Na ultrassonografia com doppler é possível detectar a cicatriz central e seu padrão radiado arterial.
A tomografia computadorizada revela, na fase sem contraste, uma imagem de massa isodensa ou moderadamente hipodensa e uma cicatriz central hipodensa com seus septos fibróticos, visualizada em um terço dos casos. Na fase contrastada, o realce do nódulo é precoce no tempo arterial, devido à sua rica e anômala vascularização arterial, e decai nas fases portal e tardia, tornando-se isodensa ou levemente hiperdensa se comparada com o parênquima adjacente normal. A cicatriz central, ao contrário, sofre um aumento do realce durante as fases tardias, tornando-se hiperdensa, consequência da impregnação de contraste em seu estroma (Figura 1).
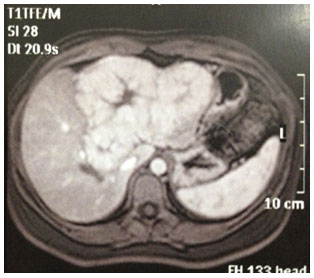
Figura 1. Tomografia evidenciando volumosa hiperplasia nodular focal em fígado esquerdo, verificar evidente cicatriz central.
A ressonância nuclear magnética permite diferenciar a HNF da adenoma hepatocelular com maior precisão, o que torna este método o de escolha para estudar essas lesões. Os nódulos de HNF são isointensos ou hipointensos nas ponderações T1 e isointenso ou moderadamente hiperintenso nas ponderações T2. A cicatriz central é hipointensa em T1 e fortemente hiperintensa em T2, uma característica que a destaca do nódulo e facilita o diagnóstico. Contudo, em apenas 50-70% dos casos, a cicatriz central é bem visualizada nos nódulos de tamanho moderado a grande (> 3cm).
Na ressonância magnética com difusão, os valores dos coeficientes que discriminam o potencial de uma lesão ser benigna ou maligna são similares para HNF, adenoma hepatocelular, metástases e carcinoma hepatocelular, limitando com isso a utilização deste método. O uso de contraste hepatobiliar específico, como gadobenate dimeglumine, pode, na ponderação T1 tardia, mostrar um nódulo de HNF hiper ou isointenso em 97%, enquanto que o adenoma hepatocelular aparece hipointenso em 100% dos casos.
A natureza da HNF é benigna, sem risco de malignização e geralmente assintomática. Quando bem diagnosticada, não tem indicação de tratamento cirúrgico ou acompanhamento clínico, salvo nos casos sintomáticos com dor ou compressão (náuseas, vômitos, plenitude) (Figura 2). Quando o diagnóstico não é firmado, torna-se necessário complementar o estudo com biópsia ou ressecção cirúrgica do espécime. O acompanhamento clínico e o manuseio destas lesões pode ser realizado de forma similar aos hemangiomas hepáticos.
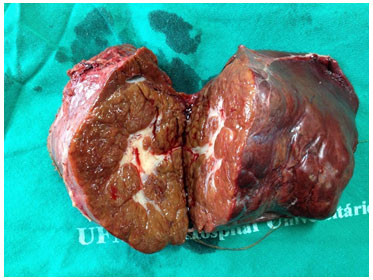
Figura 2. Peça operatória de volumosa hiperplasia nodular focal que produzia sintomas de compressão.
Adenoma hepatocelular
O adenoma hepatocelular é um tumor de origem epitelial mais comum em mulheres na idade fértil, tem associação com o uso de estrogênios, principalmente do uso de contraceptivos orais e que pode complicar com sangramento por ruptura tumoral ou transformação maligna. Pode estar associado à gravidez, uso de esteroides anabolizantes, doença do depósito de glicogênio e anomalias vasculares. Quando existe dez ou mais adenomas, denominamos adenomatose hepática. A suspensão do contraceptivo oral pode reduzir o tamanho da lesão. São mais comumente observados no lobo direito.
Podem ser classificados em Grupo 1, adenomas do gene HNF1α (Fator nuclear hepatocitário 1 alfa), observado em 35-40% dos adenomas e menos de 5% de transformação maligna. O sangramento é a maior complicação. Grupo 2, adenomas com mutação do gene β-Catenina, observado em 10-15% dos adenomas, apresentando maior predisposição para transformação maligna. Grupo 3, adenomas inflamatórios, representa 25-35% dos adenomas. Observado em obesos, sinais de síndrome metabólica e consumo de bebidas alcoólicas. Apresenta menor risco para transformação maligna, sendo o sangramento a principal complicação. Grupo 4, adenomas não classificados, representando 5-10% dos adenomas.
Normalmente são assintomáticos ou apresentam dor e desconforto no epigastro. Podem apresentar sinais de hemorragia como complicação. Considerar que acometem principalmente mulheres, entre a terceira e quinta décadas em uso de contraceptivo oral por tempo geralmente superior a cinco anos. Geralmente são achados incidentais. A função hepática está normal. O exame de imagem (tomografia computadorizada de abdome, com contraste) se caracteriza por lesão hipervascular, na fase arterial (Figura 1). A ressonância nuclear magnética apresenta acurácia superior por detectar gordura, necrose ou hemorragia nas lesões. O exame com contraste Primovist é útil para diferenciar com hiperplasia nodular focal.
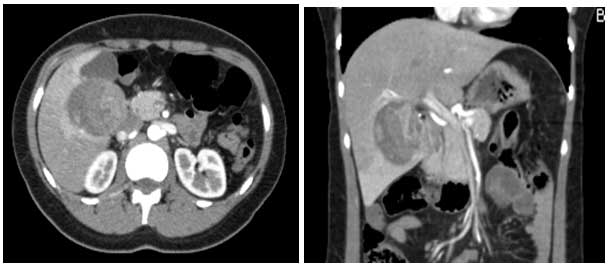
Figura 1. Tomografia com contraste (fase arterial) evidencia adenoma hepatocelular com sinais de hemorragia. A) axial; B) coronal.
O impacto da doença está relacionado ao risco de hemorragia (25% dos pacientes), transformação maligna (4% dos pacientes) e complicações durante a gravidez. Na transformação maligna, estima-se que seja principalmente em tumores maiores que cinco cm. A prevalência de transformação maligna é até dez vezes mais frequente em homens.
O tratamento consiste na interrupção do contraceptivo oral e seguimento com exames de imagem (tomografia com contraste). O controle da síndrome metabólica está indicado em adenomas do grupo 3. O tratamento cirúrgico (principalmente por videolaparoscopia, figura 2), tem sido indicado para adenomas em homens e em mulheres com tumores ≥ 5 cm, após a suspensão do contraceptivo oral. Em raros casos tem sido indicado o transplante de fígado, principalmente em adenomatose.
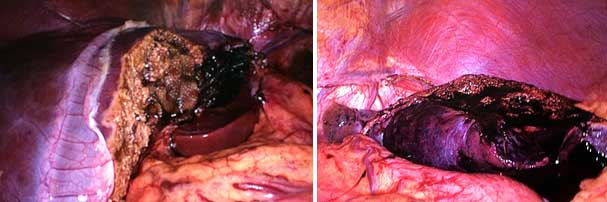
Figura 2 (A e B). Hepatectomia videolaparoscópica por adenoma hepatocelular
Carcinoma hepatocelular
O carcinoma hepatocelular é a neoplasia maligna primária mais comum do fígado. Tem sido observado um aumento de sua incidência no mundo, não apresentando sinais clínicos específicos em sua fase inicial. É mais comum no sexo masculino e geralmente acontece em pacientes com doença hepática crônica (cirrose hepática por hepatite vírus B, C e alcoólica), porém pode ser observado em fígado previamente sadio. A sequência hepatite aguda, hepatite crônica, cirrose e carcinoma hepatocelular é bem conhecida.
Por não apresentarem sintomas específicos, o diagnóstico pode ser feito apenas em pacientes cirróticos ou com alguma complicação. Nestas situações observa-se dor no hipocôndrio direito, aumento do fígado (massa abdominal palpável), emagrecimento, anorexia (falta de apetite), náuseas, vômitos, ascite (água no abdome). O diagnóstico pode ser feito através da ultra-sonografia, tomografia computadorizada e ressonância magnética do abdome superior (com enfoque ao fígado). A ressonância magnética é superior em casos de tumores menores (< 2 cm). Os marcadores virais de hepatite (HBsAg, Anti HCV) podem contribuir para o diagnóstico de carcinoma hepatocelular por apresentar relação com a doença hepática crônica. O marcador tumoral alfa fetoproteina (AFP) tem sido utilizado por muitos para o diagnóstico.
O tratamento do carcinoma hepatocelular pode ser realizado através de cirurgia (hepatectomia ou transplante hepático) ou com medidas não cirúrgicas (quimioembolização, ablação por radiofrequência). Muitos fatores podem contribuir para o prognóstico. Entre eles, o estado geral do paciente (classificação de CHILD), presença de doença extra-hepática e outros).
Metástases
O fígado é o segundo principal local de metástases (doença longe do local de origem) de câncer, precedido apenas pelos linfonodos. Por muito tempo, os pacientes com neoplasias malignas e doença metastática para o fígado foram considerados não tratáveis. Com a melhora das condições de tratamento intensivo, padrão de anestesia, refinamento da técnica cirúrgica, instituição do cirurgião com treinamento em cirurgia de fígado, isto tem mudado e os benefícios tem sido satisfatórios.
As metástases hepáticas podem ter sua origem em diferentes locais do organismo, entretanto alguns merecem destaque pelos melhores resultados cirúrgico. As mais comuns são as metástase de tumores colo-retais, tumores neuroendócrinos, câncer de mama, tumores renais, tumores supra-renais, leiomiossarcoma, melanoma e outros.
O diagnóstico das metástases é realizado através de ultra-sonografia, tomografia computadorizada com contraste oral e venoso e ressonância magnética de abdome superior. Deve ser identificado o número de metástases, sua localização, tamanho, relação com os vasos hepáticos e a presença de doença extra-hepática. A presença de ascite, carcinomatose peritoneal, implantes pélvicos, por exemplo, inviabilizam o tratamento proposto. Da mesma forma o tipo de tratamento realizado para a doença de base (colectomia com linfadenectomia, por exemplo), são importantes no resultado. Da mesma forma, o tempo de aparecimento da metástase em relação com a cirurgia anterior pode modificar o resultado.
O tratamento pode ser realizado no mesmo tempo da doença primária (no caso de alguns tumores colo-retais) ou em tempo separado. A quimioterapia pode ser realizada antes e/ou depois da cirurgia proposta. As cirurgia realizadas são as ressecções hepáticas, podendo ser associado a outros tratamentos (radiofrequência, por exemplo). Os resultados dependem de diferentes fatores.
VIAS BILIARES
- Litíase biliar (cálculos na vesícula)
- Colecistite
- Lesões polipóides da vesícula (pólipos)
- Câncer da vesícula biliar
- Litíase da via biliar (cálculos no colédoco)
- Colangite
- Estenoses da via biliar
- Colangiocarcinoma
- Tumor de papila de Vater
Colelitíase (cálculos da vesícula biliar)
Os cálculos da vesícula biliar são formados principalmente de colesterol, pigmentos biliares e mistos. Os principais fatores envolvidos na formação dos cálculos são os fatores genéticos, ambientais, idade, sexo e hormônios, paridade, obesidade, hiperlipidemias, diabetes, cirurgias, doenças hemolíticas, parasitoses. Os pacientes podem não apresentar sintomas ou cursarem com dor abdominal, geralmente contínua, no quadrante superior direito do abdome, na região epigástrica, durando mais de meia hora, podendo irradiar para as costas ou ombro direito. Pode estar relacionada com a ingestão de alimentos gordurosos. O diagnóstico geralmente é feito utilizando a ultra-sonografia de abdome superior. Podem ser observados cálculos múltiplos ou apenas um único cálculo. Os microcálculos e a lama biliar (ou barro biliar) podem ser sintomáticos e apresentar complicações.
As principais complicações da presença de cálculos na vesícula biliar são a colecistite (inflamação da vesícula), coledocolitíase (migração do cálculo para o ducto colédoco), colangite aguda (inflamação da via biliar comum, com dor, febre com calafrio e icterícia), pancreatite aguda (inflamação do pâncreas) e câncer da vesícula biliar.
O tratamento é através de cirurgia. A cirurgia é a colecistectomia videolaparoscópica, procedimento minimamente invasivo. Com três ou quatro incisões de 5 mm e 10 mm, a vesícula biliar contendo os cálculos é retirada. O curso pós-operatório geralmente é sem intercorrências e o paciente recebe alta hospitalar entre 12 e 24 horas após o procedimento cirúrgico.
Câncer da vesícula biliar
O câncer da vesícula é a neoplasia maligna mais comum da via biliar. Frequentemente é diagnosticado após a apresentação dos sintomas que são tardios. A colelitíase (cálculos na vesícula biliar) é de longe o principal fator de risco. Outras causas são as lesões polipóides da vesícula biliar, anomalias da junção do ducto bilio-pancreático, cisto de colédoco, vesícula em porcelana, obesidade, tabagismo.
Na fase inicial, o diagnóstico é difícil devido à ausência de sintomas clássicos. Em pacientes com litíase, os sintomas são da doença de base. O paciente pode apresentar dor abdominal, náuseas, vômitos, icterícia (olhos amarelados), febre, anorexia (falta de apetite), perda de peso. Em casos de suspeita da doença, a ultra-sonografia deve ser o primeiro exame a ser solicitado. A tomografia computadorizada e a ressonância magnética de abdome superior são úteis para identificar a lesão e pesquisar metástases (doença distante). Na fase avançada pode ser observada ascite (líquido no abdome), implantes peritoneais (carcinomatose) e metástases no fígado. O melhor momento de diagnóstico é na fase incidental (exame da vesícula de rotina durante a colecistectomia por colelitíase), pois a possibilidade de cura é bem maior.
O tratamento depende do estadiamento (fase evolutiva da doença). Naqueles com indicação curativa a cirurgia consiste em hepatectomia (segmento IVb e V), linfadenectomia, ressecção da via biliar (quando invade o ducto cístico). O tratamento paliativo pode ser através de endoscopia, radiologia intervencionista ou cirurgia, associado à quimioterapia.
O prognóstico depende do estadiamento da lesão e da resposta ao agente quimioterápico.
PÂNCREAS
As principais doenças cirúrgicas do pâncreas são:
1. Pancreatite
- Aguda
- Crônica
2. Neoplasias
- Císticas
- Sólidas:
- Câncer do pâncreas
Pancreatite aguda
A pancreatite aguda é uma doença inflamatória causada pela digestão do parênquima pancreático por suas próprias enzimas, com envolvimento variável de tecidos peri-pancreáticos e de sistemas orgânicos distantes. A pancreatite aguda apresenta como principais causas a litíase biliar (cálculos da vesícula biliar), álcool, alterações anatômicas (pâncreas divisum), procedimentos endoscópicos (CPRE-colangiopancreatografia retrógrada endoscópica), trauma, pós-operatório, infecções.
Clinicamente o paciente apresenta dor epigástrica (ou em barra) ou no abdome superior (ou ainda dor lombar), náuseas, vômitos. Pode ainda apresentar febre, taquicardia (aumento da freqüência cardíaca), distensão abdominal, icterícia (olhos amarelados). O diagnóstico é realizado através de exames de laboratório e exames de imagem. A amilase e lípase séricas (no soro) estão aumentadas e o hemograma pode evidenciar leucocitose (aumento das células brancas do sangue). A glicemia (glicose no sangue) está aumentada. O exame de imagem utilizado é a tomografia computadorizada do abdome que deve ser realizada com contraste.
Normalmente o tratamento é clínico. O paciente deve ser internado e observado os cuidados de manutenção do estado geral do paciente. Em caso de pancreatite grave (severa) o tratamento deve ser realizado em Unidade de Terapia Intensiva (UTI). A base do tratamento é a manutenção dos sinais vitais com reposição volêmica, analgésicos, controle das complicações. A cirurgia está indicada em casos complicados (necrose infectada, pseudocistos) e quando não há melhora apesar das medidas clínicas satisfatórias. Naqueles de etiologia biliar a colecistectomia deve ser realizada após a segunda semana de doença, quando há melhora do quadro, ainda com o paciente internado.
Câncer do pâncreas
A neoplasia primária mais comum do pâncreas é o adenocarcinoma ductal do pâncreas. A maioria se origina na cabeça. O processo de manifestação mais comum está relacionado com fatores genéticos e ambientais. Outros fatores são a idade, tabagismo, pancreatite crônica, ingestão de gorduras, diabetes tipo II, entre outros. A manifestação clinica pode ser através de icterícia (olhos amarelos), nos tumores de cabeça de pâncreas, perda de peso, dor abdominal, dispepsia. Entre os exames laboratoriais podem ser observados o aumento das bilirrubinas, fosfatase alcalina, Gama GT e anemia. O marcador CA 19-9 pode contribuir tanto para o diagnóstico quanto para evolução do tratamento. A tomografia computadorizada do abdome superior, com contraste oral e venoso, bem como a ressonância nuclear magnética são úteis para o diagnóstico, evidenciando a lesão e verificando a presença de metástases, invasão de vasos e presença de ascite (líquido no abdome). O tratamento cirúrgico com finalidade curativa acontece em aproximadamente 20% dos casos. A cirurgia é a duodenopancreatectomia com linfadenectomia (Operação de Whipple). O tratamento paliativo da icterícia acontece através da endoscopia (CPRE-colangiopancreatografia retrógrada endoscópica) com uso de próteses ou com cirurgia através da derivação bilio-entérica. Nestes casos o prognóstico é reservado.
PAREDE ABDOMINAL
- Hérnia:
- Inguinal
- Crural (Femoral)
- Umbilical
- Incisional (Pós-operatória)
Hérnia inguinal
As hérnias inguinais podem ser diretas ou indiretas (obliqua externa). As hérnias indiretas acompanham os elementos do cordão espermático (ou ligamento redondo na mulher). Podem se manifestar como simples protusão na região inguinal (caroço) relacionado com o esforço e que reduz com o repouso, ou acompanhar os elementos do cordão espermático em direção à bolsa escrotal (hérnia ínguino-escrotal). Podem ser redutíveis (retornam à cavidade de forma espontânea), ou irredutíveis do tipo encarcerada ou estrangulada (esta é uma condição de emergência por haver comprometimento vascular). Da mesma forma a hérnia pode ser unilateral (direita ou esquerda) ou bilateral.
O diagnóstico é clínico com o paciente apresentando dor e aumento de volume na região inguinal (ou bolsa escrotal), relacionado com um esforço físico (pode acontecer com o ato de defecar, em prostáticos, esforço da tosse, entre outras). As manobras de esforço na região inguinal podem fazer o diagnóstico.
O tratamento é através de cirurgia que pode ser realizada por via aberta (convencional) ou por videolaparoscopia. As técnicas podem ser com tensão (tipo técnica de Bassini), ou sem tensão (chamadas Tension free) como a técnica de Lichtenstein. As técnicas sem tensão usam próteses (chamadas de telas ou malhas) que substituem a parede da região inguinal. Os índices de recidiva (retorno da hérnia após o tratamento) são menores com as técnicas livre de tensão. A anestesia pode ser local, peridural, raquianestesia ou anestesia geral.